Nghiên cứu điều chế thuốc phóng xạ 18F-Sodium fluoride và 32P-Chromic phosphate
Ngày đăng: 01/04/2025 14:42
Hôm nay: 0
Hôm qua: 0
Trong tuần: 0
Tất cả: 0
Ngày đăng: 01/04/2025 14:42
Y học hạt nhân là chuyên ngành sử dụng các đồng vị phóng xạ (ĐVPX) để nghiên cứu, đánh giá các quá trình sinh bệnh lý và chuyển hóa của cơ thể nhằm mục đích chẩn đoán và điều trị. Các ĐVPX sử dụng để tạo nên dược chất phóng xạ (DCPX) hay gọi là thuốc phóng xạ (radiopharmaceutical). Các thuốc phóng xạ được sản xuất từ công nghệ lò phản ứng hạt nhân, máy gia tốc cyclotron và các bình phát xạ (generator). Ở Việt Nam thuốc phóng xạ đã được sử dụng từ lâu, tuy nhiên chúng được quản lý theo chuyên mục hóa chất.
 |
Từ năm 2017, thông tư 20 của Bộ Y tế được ban hành thì các thuốc này mới được quản lý theo chuyên mục thuốc phóng xạ. Việc sản xuất, nghiên cứu tự sản xuất các thuốc phóng xạ trong nước còn nhiều hạn chế do phụ thuộc vào trang thiết bị, nguồn nhân lực... Tuy nhiên, trong những năm gần đây, lĩnh vực này đã và được các bộ ngành quan tâm để thúc đẩy khả năng tự đảm bảo nguồn cung thuốc phóng xạ trong nước.
Kỹ thuật PET là một kỹ thuật hiện đại trong y học hạt nhân và lần đầu tiên được sử dụng trong lâm sàng ở Việt Nam từ hơn một thập kỷ qua. Sau hơn 10 năm, số lượng máy gia tốc và số lượng máy PET ở Việt Nam tăng khá nhanh nhưng hiện nay chúng ta mới chỉ triển khai được kỹ thuật ghi hình PET với 18F-FDG. Mặc dù 18F-FDG vẫn là DCPX phổ biến nhất để ghi hình PET.
Tuy nhiên, DCPX này là loại không đặc hiệu từng loại ung thư và với cơ quan nên có thể dương tính giả do 18FFDG hấp thu tăng ở các vị trí viêm hay các cơ quan tổ chức sau phẫu thuật hoặc âm tính giả với các khối u ở các cơ quan, tổ chức không tăng chuyển hoá đường… Chính vì vậy cần phải có các DCPX có cơ chế hấp thu, chuyển hóa và nhắm các đích, cơ quan khác ngoài 8 F-FDG để khắc phục những hạn chế của 18F-FDG PET. 18F-sodium fluoride (Na18F) là một DCPX sử dụng để ghi hình PET đặc hiệu với tổ chức xương và được sử dụng trong chẩn đoán ung thư xương nguyên phát, di căn xương và một số các bệnh lý xương khớp khác. DCPX này có nhiều ưu điểm hơn 99mTc-MDP là DCPX sử dụng ghi hình xạ hình xương kinh điển trên máy gamma camera SPECT do nó hấp thu nhanh và tập trung cao ở xương. Sử dụng Na18F PET/CT tăng độ nhạy và độ đặc hiệu chẩn đoán hơn hẳn kỹ thuật xạ hình xương thông thường trên máy gamma camera. Tuy nhiên, do 18F-NaF có thời gian bán rã ngắn (110 phút) nên không thể nhập khẩu mà chỉ có thể tổng hợp ở các cơ sở có máy gia tốc ở trong nước.
Hiện nay, ở Việt Nam thuốc phóng xạ Na18F chưa được đưa vào ứng dụng trong lâm sàng. Từ năm 2009, Trung tâm máy gia tốc 30 MeV tại Bệnh viện TƯQĐ 108 chính thức đi vào hoạt động. Dự án này nhằm phát triển các ngành khoa học kỹ thuật có sử dụng bức xạ hạt nhân, đặc biệt là trong y tế tại Việt nam. Trong lĩnh vực y học, máy gia tốc là một công cụ không thể thiếu để sản xuất ra các đồng vị phóng xạ cho điều chế các dược chất phóng xạ (DCPX) cho kỹ thuật ghi hình phát bức xạ positron (positron emission tomography - PET).
Từ những phân tích về điều kiện cơ sở vật chất sẵn có, những ưu điểm và tiềm năng ứng dụng trong lâm sàng của thuốc phóng xạ 18F-Sodium fluoride và thuốc phóng xạ 32P-Chromic phosphate cũng như góp phần thúc đẩy ứng dụng các đồng vị phóng xạ trong y học trong chương trình KC.10/16-20. Chủ nhiệm đề tài PGS.TS Lê Ngọc Hà cùng nhóm nghiên cứu tại Bệnh viện trung ương quân đội 108 thực hiện đề tài “Nghiên cứu điều chế thuốc phóng xạ 18F-Sodium fluoride và 32P-Chromic phosphate” với mục tiêu: Xây dựng quy trình và điều chế thuốc phóng xạ 18F-Sodium fluoride (Na18F) đạt tiêu chuẩn Dược điển Anh 2018; Xây dựng quy trình và điều chế thuốc phóng xạ 32P-Chromic phosphate (Cr32PO4) đạt tiêu chuẩn Dược điển Mỹ 41; Đánh giá được tính an toàn, hiệu quả chẩn đoán của Na18F và hiệu quả điều trị của Cr32PO4 trên động vật thực nghiệm.
Sau thời gian nghiên cứu, đề tài đã thu được những kết quả như sau:
Nghiên cứu điều chế thuốc phóng xạ Na18F:
Nhóm nghiên cứu đã thiết kế và chế tạo được module tổng hợp DCPX 18F–NaF tự động trên bộ kít sử dụng một lần cho quy mô 1000 mCi/mẻ và hiệu suất tổng hợp > 90%.
Xây dựng hoàn chỉnh quy trình tổng hợp thuốc phóng xạ Na18F tự động trên module tự thiết kế chế tạo của nhóm nghiên cứu KC.10.37/16-20.
Xây dựng quy trình kiểm tra chất lượng Na18F theo tiêu chuẩn chất lượng của Dược điển Anh 2018. Các mẻ thuốc đều đạt yêu cầu và ổn định trong vòng 8 giờ.
Khảo sát được phân bố phóng xạ của Na18F trên chuột cho thấy thời gian ghi hình PET/CT là 45 phútsau khi tiêmlà hợp lý vì khi đó tỷ lệ hấp thu xương/phôngcơ thể là cao nhất. Hình ảnh Na18F PET/CT rõ ràng, sắc nét hơn hẳn so với 99mTc-MDP SPECT trên thỏ. Thuốc Na18F không thấy gây độc tính cấp trên chuột với liều quy đổi gấp 100 lần liều trên người. Các kết quả thu được cho thấy thuốc phóng xạ Na18F rất có tiềm năng ứng dụng trong lâm sàng.
Nghiên cứu điều chế phóng xạ Cr32PO4
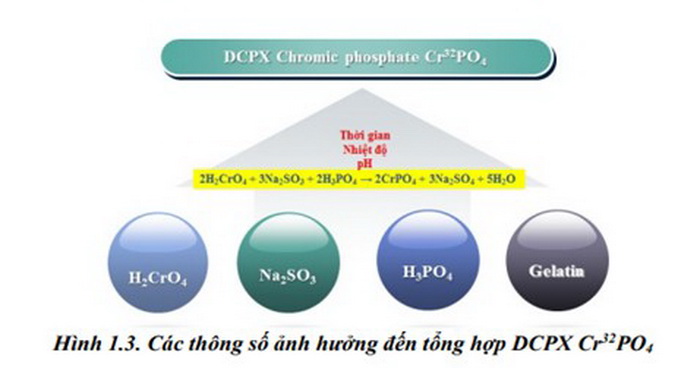
Điều chế đồng vị 32P dạng dung dịch H3 32PO4 từ bia 32P2O5 và bia 32S trên lò phản ứng hạt nhân Đà Lạt. Tổng hợp thành công dược chất phóng xạ Cr32PO4 với hiệu suất tổng hợp khá cao (khoảng 86%). Chất lượng dược chất phóng xạ Cr32PO4 đạt tiêu chuẩn theo dược điển Mỹ 41 (USP41).
Kết quả phân bố sinh học trên chuột thí nghiệm cho thấy Cr32PO4 tập trung trong gan với mức từ 2 - 17 ID%/g trong vòng 6 giờ sau khi tiêm và giảm dần theo thời gian cho đến 336 giờ còn khoảng 5 ID%/g. Kết quả kiểm tra đào thải trên chuột cho phân bố DCPX trong thận tăng lên sau một ngày tiêm cho thấy thuốc có đào thải qua thậ n. DCPX giảm dần qua thận theo thời gian theo dõi cho đến 336 giờ. DCPX đào thải ra khỏi máu và bài tiết qua thận nhanh, sau 24 giờ tiêm là lượng DCPX qua thận giảm dần và thuốc.
Kết quả đánh giá độc tính cấp của Cr32PO4 được điều chế tại Viện hạt nhân Đà Lạt trên chuột của chúng tôi cho thấy Cr32PO4 có làm thay đổi một số chỉ số huyết học và một số chỉ số hoá sinh. Kết quả giải phẫu bệnh lí cơ bản hai nhóm chứng và điều trị không có sự khác biệt. Đây là các tác động thường thấy của các dược chất phóng xạ với liều Cr32PO4 liều 17,1 mCi/kg sau 2 và 14 ngày.
Kết quả đánh giá tác dụng điều trị sau 2 tuần cho thấy thuốc Cr32PO4 đã làm giảm kích thước khối u đáng kể (21,92%) và sau khoảng 5 chu kỳ điều trị liên tiếp bằng Cr32PO4 thì khối u ung thư tuyến tiền liệt sẽ giảm hoàn toàn.
Có thể tìm đọc toàn văn báo cáo kết quả nghiên cứu (mã số 20752/2022) tại Cục Thông tin khoa học và công nghệ quốc gia.
Vnexpress